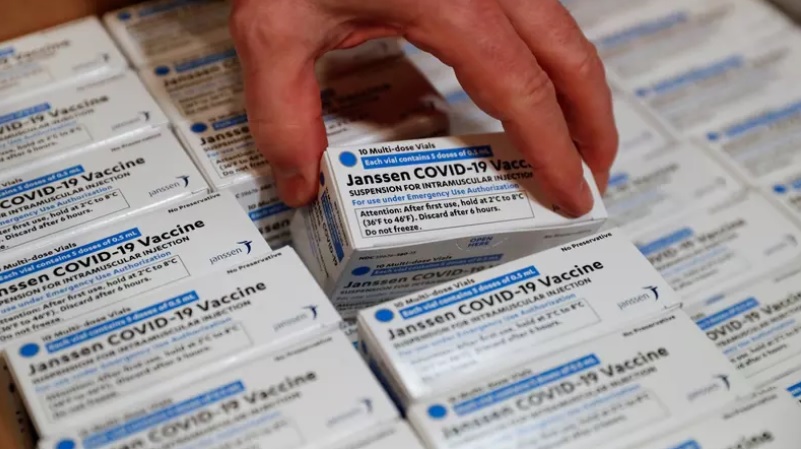
Por unanimidade, a Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quarta-feira, 31, o uso emergencial da vacina da Janssen, braço farmacêutico da Johnson & Johnson, contra a Covid-19 no Brasil. Com a decisão, a vacina pode agora ser aplicada na população brasileira.
A entrega de 38 milhões de doses do imunizante, que faz parte do Plano Nacional de Imunizações (PNI) do Ministério da Saúde, deve começar em julho – até setembro, devem ser entregues 16,9 milhões de doses; depois, de outubro a dezembro, são esperadas mais 21,1 milhões de doses.
A diretora da Anvisa, Meiruze Souza Freitas, relatora do pedido, ressaltou que a vacina da Janssen já foi aprovada para uso emergencial pelas agências americana, canadense e europeia, além da Organização Mundial da Saúde (OMS).
"Dada a atual situação de emergência, considera-se que as incertezas podem ser resolvidas por meio de obrigações específicas, incluindo a continuação do estudo clínico principal pelo maior tempo possível, estudo de eficácia após aprovação e vigilância de rotina de segurança. A vacina atende as expectativas dessa agência quanto as requisitos de qualidade, segurança e eficácia para autorização dessa vacina no contexto do uso emergencial", afirmou.
Deixe o seu comentário